

资讯动态
neotrident news
资讯动态
讲座主题:从分子到记忆:阿尔茨海默病与药物设计
讲座时间:2024年5月30日(周四),14:00
报名方式:扫描下方二维码 或


进入直播间,打开后记得收藏
阿尔茨海默病(alzheimer’s disease, ad)是一种复杂的神经退行性疾病,它会逐渐剥夺患者的记忆和认知能力。随着全球人口的老龄化,ad的发病率不断上升,成为全球公共卫生的重大挑战。尽管科学家们在理解和治疗这种疾病方面取得了一些进展,但ad的药物设计仍然充满挑战。
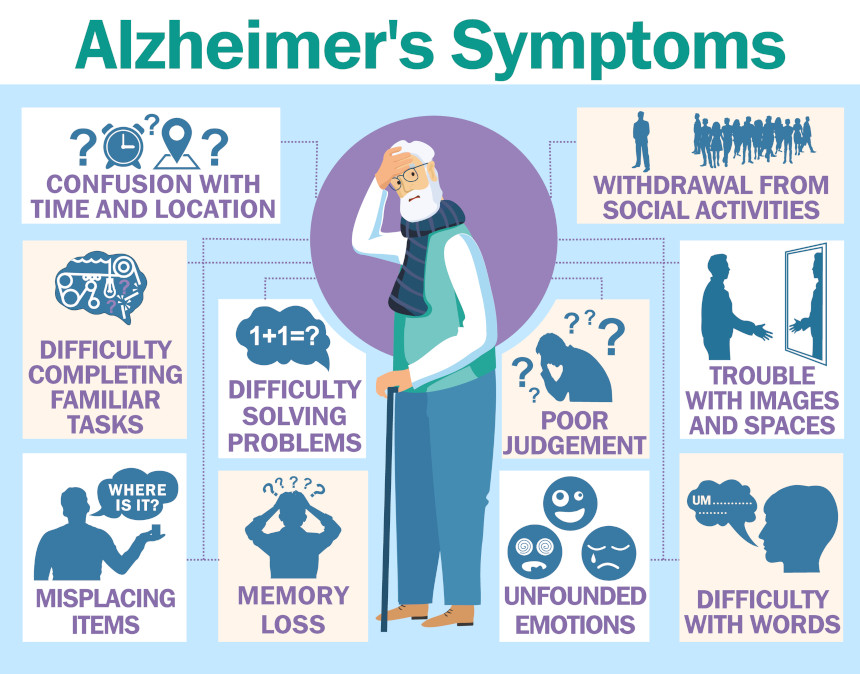
图 | 阿尔茨海默病症状
(来源:https://www.saturdayeveningpost.com/2020/09/world-alzheimers-month-the-mind-of-the-matter/)
从分子层面上,ad的发病机制至今未完全明了,但广泛认为与β-淀粉样蛋白(aβ)的异常沉积和tau蛋白的异常聚集有关。这些分子变化导致神经细胞功能受损和死亡,进而引发记忆和认知障碍。其中,aβ蛋白是由淀粉样前体蛋白(app)经过切割产生的,其异常沉积形成的斑块是ad的标志性病理特征。aβ蛋白的聚集不仅损害神经细胞,还能激发炎症反应,进一步加剧病情。tau蛋白则是微管结构的稳定因子,但在ad中,异常的tau蛋白会形成神经纤维缠结,破坏神经细胞内部的运输系统,导致细胞功能障碍和死亡。
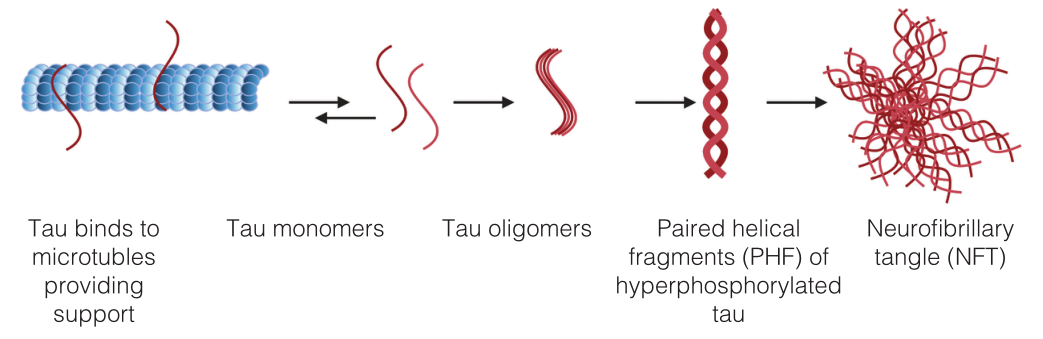
图 | tau聚集导致神经原纤维tau缠结
(来源:huang x, ed. alzheimer’s disease: drug discovery. brisbane (au): exon publications; december 18, 2020.)
目前针对ad的药物设计主要集中在两个方向:一是开发能够阻止或逆转aβ和tau蛋白异常沉积的药物;二是寻找能够改善神经细胞功能和延缓病程的药物。近年来,许多研究集中在开发针对aβ和tau蛋白的药物。例如,aducanumab是一种针对aβ蛋白的单克隆抗体,它可以帮助清除脑中的aβ斑块。然而,这类药物的临床试验结果并不一致,有些药物未能显示出预期的治疗效果。除了直接靶向ad的分子病理特征外,科学家们也在探索能够提供神经保护和功能改善的药物。这些药物可能通过抗炎、抗氧化或改善神经细胞代谢等机制发挥作用。
从分子到记忆,阿尔茨海默病的治疗需要跨学科的合作和创新思维。虽然目前还没有根治ad的药物,但随着科学技术的进步,特别是cadd和ai技术的应用,未来有望开发出更有效的治疗方法。科学家们正不懈努力,希望能够为ad患者带来光明的未来。
创腾科技的maxflow平台可以利用分子模拟和人工智能技术实现抗阿尔茨海默病的药物设计:
1、利用虚拟筛选技术,使用分子对接和药靶亲和力预测模型,进行基于靶点的药物设计。分子对接能模拟小分子与特定生物靶标之间的相互作用,计算氢键、范德华力以及疏水性相互作用等分子间的关键作用力,从而确保选出的分子能够以高度特异性和亲和力与目标靶点结合。基于深度学习算法的药靶亲和力预测模型,能够综合考虑包含多种理化性质和生物信息学的训练数据,预测出化合物与靶蛋白之间的结合自由能,从而评估分子作为候选药物的可能性及其效力。
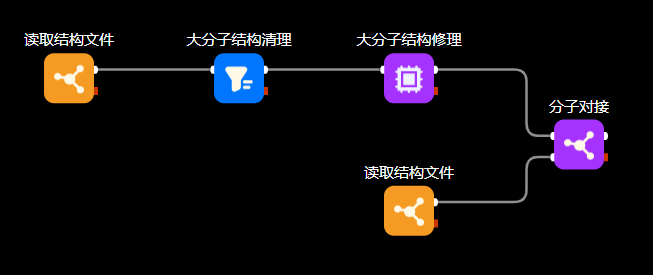
图 | 分子对接工作流
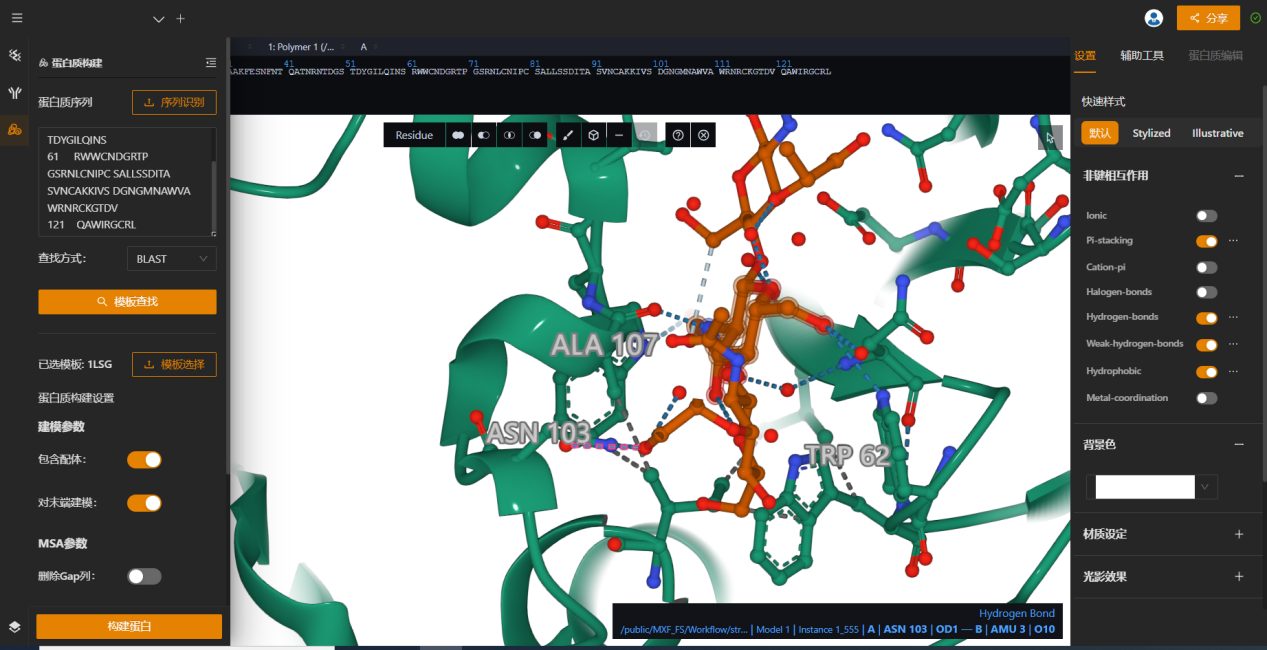
图 | 靶点结构构建页面
2、 利用admet性质预测模型,预测化合物的血脑屏障通透性。基于该预测模型,研究者能够在庞大的化合物库中快速筛选出具有理想admet属性的分子结构,加速药物发现的早期阶段,减少实验成本和时间。
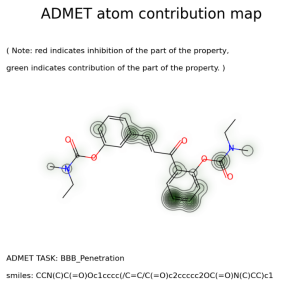
图 | 深度学习admet模型获得的原子贡献图
3、利用抗体-抗原对接功能,进行抗体药物的设计。结合ai 分子模拟我们可以利用大分子对接和md技术对突变后的候选抗体进行结构优化和相互作用分析,并模拟其与抗原的结合过程和相互作用参数,研究作用机制。也可利用ai技术根据候选抗体与目标抗原之间的相互作用位点和构象,预测可能增强或减弱相互作用强度的突变位点。这样,我们就可以优化候选抗体的结构和功能,并提高抗体药物的效果和安全性。
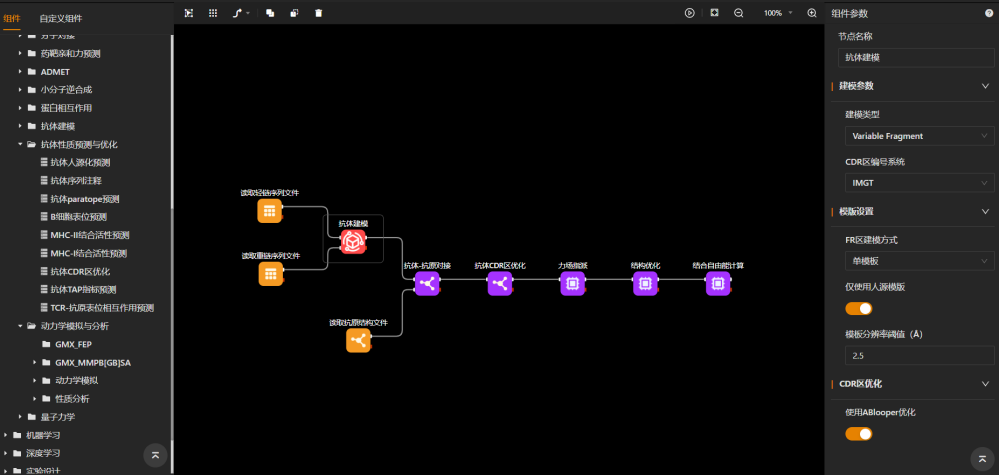
图 | maxflow平台中ai 分子模拟抗体设计工作流
创腾科技的maxflow平台还能如何助力科学家进行神经退行性疾病的药物设计?敬请关注5月30日的在线讲座